Общеизвестный факт – в естественных условиях вода может существовать только в трёх состояниях: твёрдом, жидком и газообразном. На самом деле при помощи различных факторов можно заставить воду обрести совершенно неожиданную форму. В нашей статье мы расскажем Вам о самых необычных формах и состояниях воды.

Лёд VII

В естественных условиях нашей планеты вода в твёрдом агрегатном состоянии обладает относительно низкой температурой. Исключение составляет модификация привычного льда под названием лёд VII. В отличие от обычного льда, который существует в фазе Ih и имеет гексагональную кристаллическую структуру, в модификации VII молекулы воды обретают кубическую структуру. В искусственных условиях получение кубического льда возможно при давлении 2,216 ГПа и температуре около 80 °C, однако он сохраняет свою структуру вплоть до температуры более 440 °C при давлении 10 ГПа. За счёт кубической структуры решётки этот лёд гораздо плотнее обычного.

Ранее специалистам приходилось иметь дело только со льдом VII космического происхождения либо самостоятельно создавать его в лабораторных условиях. В 2018 году учёным впервые удалось обнаружить лёд VII на Земле. Группа учёных под руководством профессора геонаук из Университета Невады Оливера Шаунера исследовала месторождение алмазов, которые являются одним из самых информативных источников данных о составе и поведении мантии Земли. В одном из алмазов, образовавшемся на глубине около 644 км под земной корой, учёные обнаружили молекулы льда VII.
Сухая вода

Противоречивое словосочетание «сухая вода» как нельзя лучше характеризует необычное сочетание молекул воды и диоксида кремния. Сухая вода была впервые получена в 1968 году и получила широкое применение в косметической индустрии. При помощи специального аппарата в лабораторных условиях создаётся вещество, которое на 95% состоит из воды. Номинально эта смесь находится в жидком агрегатном состоянии, но на самом деле она больше похожа на светлый речной песок. Дело в том, что диоксид кремния изолирует крошечные капли воды, не позволяя им смешиваться и вести себя как жидкость.
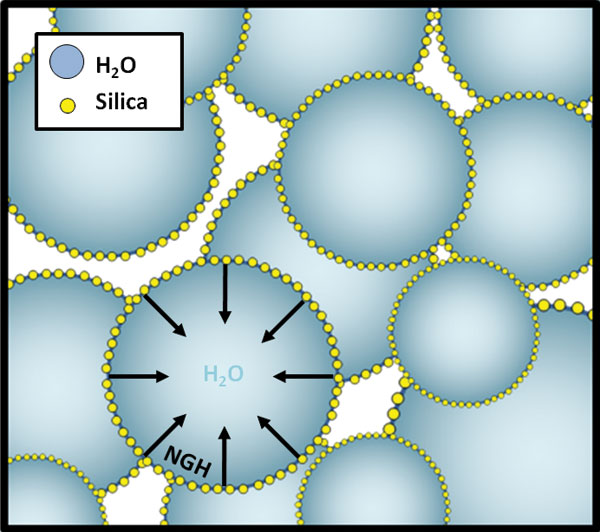
Современных учёных заинтересовала высокая впитывающая способность сухой воды. Специалисты считают, что её можно использовать для безопасной транспортировки опасных химикатов или топлива. Кроме того, водяной порошок способен активно поглощать углекислый газ – в такой форме вода аккумулирует почти в три раза больше диоксида углерода, чем в жидком. Эксперты не исключают возможности применения вещества для борьбы с глобальным потеплением, путём извлечения углекислого газа из атмосферы.
Сверхкритическая жидкость

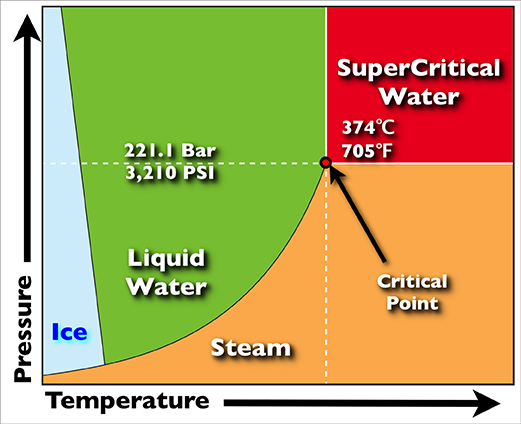
Любое вещество достигает сверхкритического состояния, если его температура и давление достигают настолько экстремального значения, что становится невозможным определить разницу между его жидким и газообразным агрегатными состояниями. Для воды этот «переломный момент» наступает при температуре 374 °C и давлении в 218 атмосфер. При этом жидкость ведёт себя как своеобразный пар, который способен проходить сквозь твёрдые тела и даже растворять некоторые из них. Свойства сверхкритической жидкости применимы в широком ряде промышленных отраслей: нефтехимической, пищевой, парфюмерной, фармацевтической и т. п.
Гидроплазма или плазма воды

В 40 световых годах от Земли в созвездии Змееносца находится уникальная экзопланета GJ 1214 b. GJ или Глизе в 6,5 раз тяжелее нашей планеты, а её поверхность и атмосфера почти полностью состоят из воды в различных агрегатных состояниях. Особое место среди них занимает плазма воды. Некоторые характеристики этого состояния – низкая плотность и отсутствие унифицированной формы – напоминают газ. Однако в отличие от газа, в плазме атомы вещества лишены своих электронов, потому положительно заряженные ядра свободно передвигаются в пространстве.

GJ 1214 b находится очень близко к своей материнской звезде – настолько, что её год длится всего 36-38 часов. Для сравнения, Земля расположена в 70 раз дальше от Солнца. Близость к звезде сильно разогревает планету, потому средняя температура её поверхности составляет 200-280 °C. Высокие температуры и давление заставляют воду сжиматься до тех пор, пока она не превращается в плазму.
Тройная точка

Тройная точка вещества определяет условия, при которых оно находится одновременно в твёрдом, жидком и газообразном состоянии. Это возможно исключительно по достижении момента так называемого термодинамического равновесия. Вода обретает это равновесие при температуре 0,01 °C и давлении 611,66 паскалей. Тройная точка воды является опорным фактором для калибровки разнообразных приборов. Также ранее её использовали для определения одной из ключевых единиц измерения температуры – кельвина.
Суперионная вода

Суперионная вода, также известная как лёд XVIII – это ещё одна фаза воды в твёрдом агрегатном состоянии, сформированная в результате резкого и значительно скачка температуры и давления. Лёд XVIII горячий, плотный материал чёрного цвета, который ведёт себя как металл. Кубик суперионного льда в четыре раза тяжелее куба обычного льда того же объёма. Многие учёные считают, что лёд XVIII – самая распространённая форма воды за пределами нашей планеты, так как она составляет львиную долю тела таких космических объектов как «ледяных гигантов», например, Урана или Нептуна.
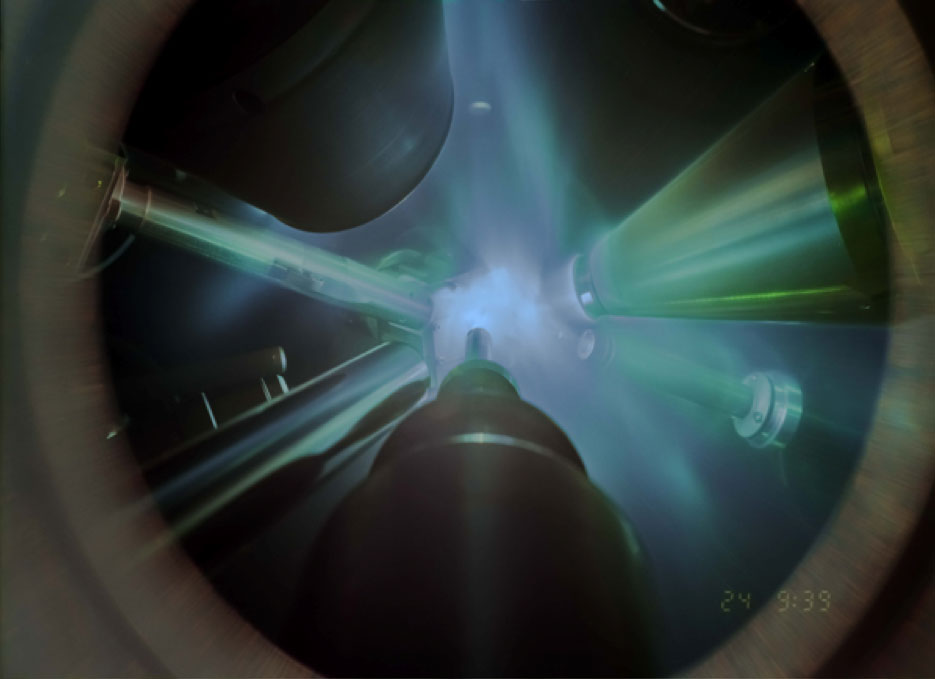
О существовании суперионной воды учёные предполагали ещё во второй половине XX века, но только в 2019 году им удалось подтвердить свои догадки. В ходе эксперимента исследователи пронзили каплю воды мощнейшим лазером. Ударные волны сформировали в воде плотную кубическую кристаллическую решётку из молекул кислорода, вокруг которых свободно передвигается жидкий водород. Некоторые специалисты считают, что лёд XVIII нельзя называть водой, так как при образовании его структуры молекулы кислорода и водорода распадаются.
Аэролёд
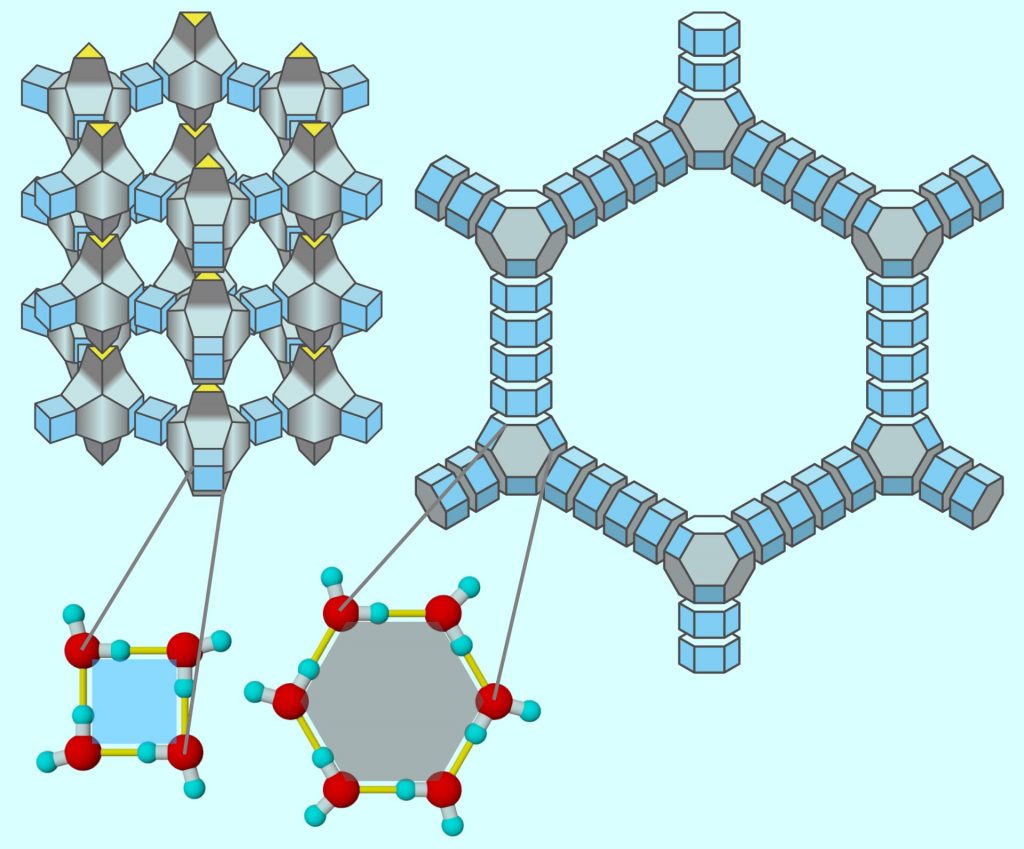
Аэролёд – это самая лёгкая и наименее плотная фаза льда. Её существования было предсказано в ходе симуляции процесса превращения воды в лёд в Университете Окаямы в Японии в 2017 году. Во время эксперимента учёные наблюдали за тем, как происходит смена агрегатного состояния в различных условиях, в том числе при негативном давлении.

При помощи компьютерного моделирования исследователи формировали разнообразные молекулярные соединения известных типов льда на основе цеолитов – микропористых минералов. Из молекулы диоксида кремния они извлекли оба атом кислорода, атом кремния заменили атомом кислорода и добавили к нему два атома водорода, получив гексагональную решётку льда на месте кристалла минерала. Затем учёные изучили свойства теоретического вещества и пришли к выводу, что аэролёд имеет меньшую плотность, чем любой из существующих видов льда. Специалисты утверждают, что это открытие может оказаться полезным для понимания того, как жидкости ведут себя в условиях космоса и других космических тел.
Аморфный лёд


При быстром охлаждении жидкой воды до температуры −137 °C формируется так называемый аморфный лёд, который не имеет чёткой кристаллической решётки. Молекулы такого льда располагаются в случайном порядке как атомы в обычном стекле. С научной точки зрения, аморфный лёд является жидкостью, молекулы которой находятся в невероятно медленном (в сравнении с обычной водой) движении. В 2017 году специалисты предположили, что аморфный лёд является промежуточной фазой между жидким и агрегатным состояниями воды.
Горящий лёд

Гидрат метана – это минерал, который представляет собой лёд с особенной кристаллической структурой. Внутри кластеров молекул воды размещаются молекулы метана или некоторые его соединения. Между собой они связаны непрочными молекулярными связями, которые легко нарушаются при повышении температуры. Гидрат метана в виде льда существует в зонах вечной мерзлоты и на дне Мирового океана. Горящий лёд можно использовать в качестве альтернативного ископаемого топлива, так как его запасы на Земле в десятки раз превышают мировые запасы нефти. Главным недостатком такого топлива является его нестабильность при повышении температуры и понижении давления. Кроме того, многие специалисты считают гидрат метана активным участником изменений климата нашей планеты, так как из-за таяния льдов происходит высвобождение метана в атмосферу.
Квантовая вода

В 2016 году специалисты Ок-Риджской национальной лаборатории США провели эксперимент, в ходе которого они изобрели новое состояние воды – квантовое. Учёные «втиснули» молекулы воды внутрь гексагональных кристаллов минерала берилла. Невероятное сжатие привело к критическому повышению давления, из-за которого молекулы стали разупорядоченными. В квантовом состоянии вода просто-напросто игнорирует ряд правил классической физики. Например, молекулы квантовой воды могут преодолевать различные барьеры на атомном и электронном уровне. В квантовой механике такое явление называется туннельным эффектом. Учёные считают, что именно квантовое состояние позволяет воде проникать сквозь различные преграды в условиях реального мира, например, сквозь стенки клеток живых организмов.

