Управление по контролю качества пищевых продуктов и лекарственных средств США впервые одобрило применение сразу двух методов генотерапии, предназначенных для лечения серповидноклеточной анемии – Lyfgenia и Casgevy. К слову, последний также является первым разрешённым методом терапии, основывающимся на технологии CRISPR/Cas9, не только для СКА, но для любых генетических заболеваний.

Серповидноклеточная анемия – это группа наследственных заболеваний крови, затрагивающих гемоглобин – железосодержащий белок, ответственный за транспортировку кислорода. Вследствие заболевания он приобретает кристаллическое строение, а несущие его эритроциты получают специфическую серпообразную форму. Хрупкость красных клеток крови приводит к их преждевременной гибели, вследствие чего у больного наблюдается постоянная анемия, а также происходит периодическая закупорка мелких сосудов в разных частях тела. Это делает пациентов со СКА подверженными повышенной утомляемости, отёкам и артриту, тромбозу и язвам, которые сопровождаются приступами боли. Актуальные методики лечения данного заболевания заключаются в предотвращении и купировании боли и осложнений вазоокклюзивных кризов.
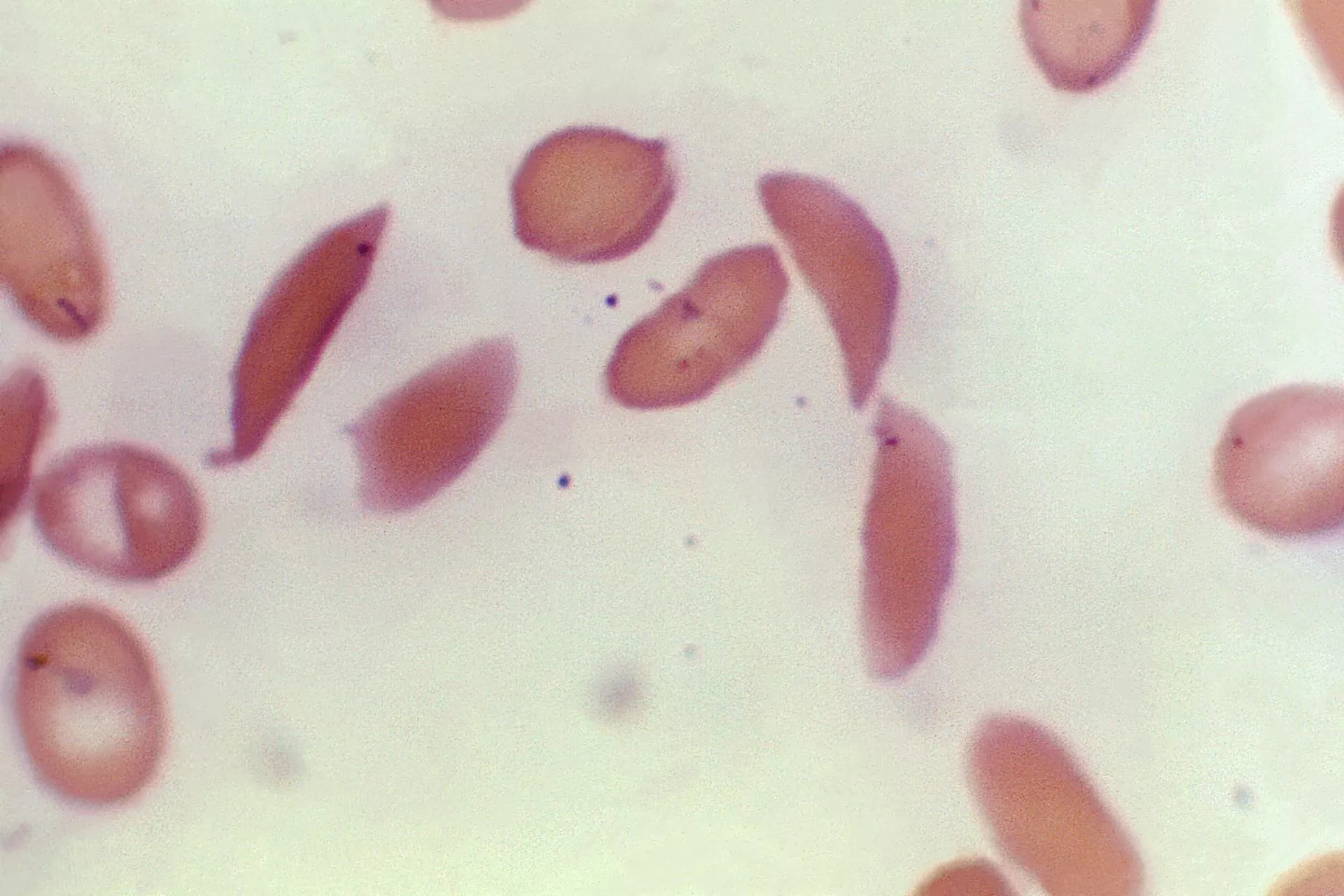
Поскольку заболевание связано с мутацией гена HBB, кодирующего β-цепь основной разновидности взрослого гемоглобина, гемоглобина А, одним из самых перспективных направлений в терапии СКА уже много лет считается генотерапия, способная заставить организм производить правильный белок либо компенсировать его функции. Разработка методов генетической терапии серповидноклеточной анемии продолжается уже более пятнадцати лет, и в ноябре 2023 года один из них впервые был одобрен в Великобритании для использования пациентами старше 12 лет (Casgevy). Спустя месяц FDA одобрило не один, но сразу два инновационных метода генотерапии – Casgevy и Lyfgenia.
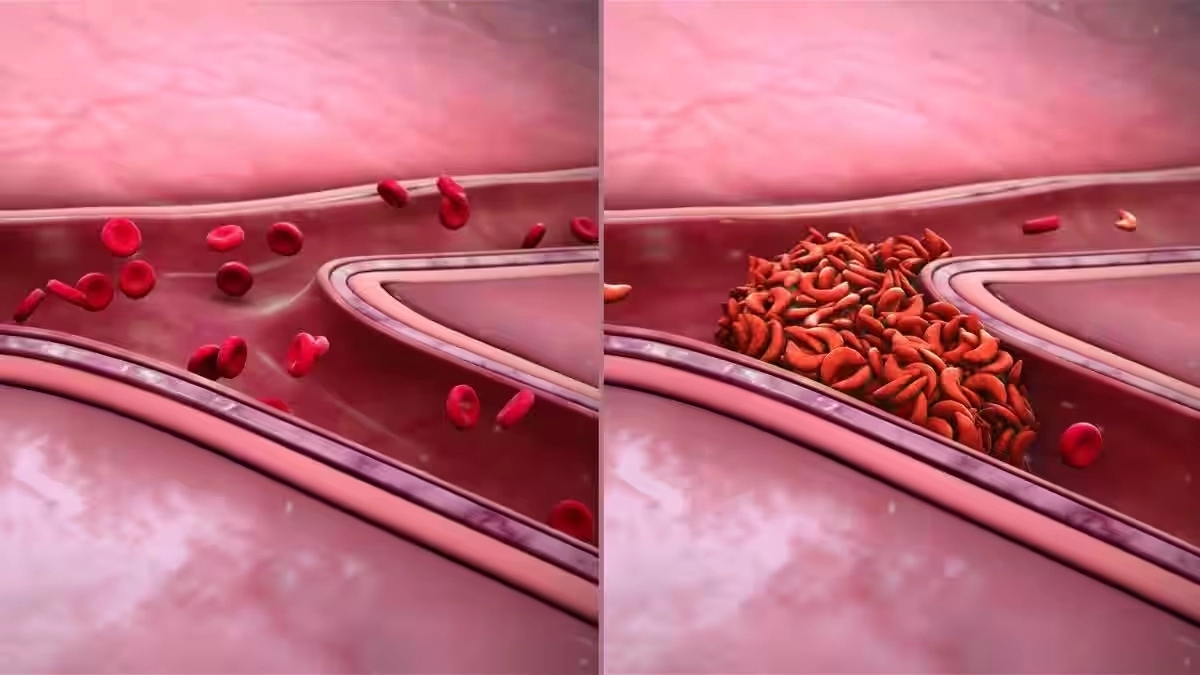
Lyfgenia использует для транспортировки исправленного гена вирусный вектор, а именно, лентивирусы, модифицированные таким образом, чтобы они не могли размножаться после первичного «заражения» клетки пациента. С помощью вектора специалисты «обучают» гемопоэтические стволовые клетки больного производить новый гемоглобин HbAT87Q, который функционирует в точности как здоровый гемоглобин А. Несущие его эритроциты с меньшей вероятностью деформируются и не затрудняют кровоток.

Casgevy – это первая одобренная FDA генотерапия, полагающаяся на технологию модификации генома CRISPR/Cas9. После обработки гемопоэтических стволовых клеток пациента при помощи данного инструмента они начинают производить повышенное количество HbF (фетального гемоглобина F). Этот белок берёт на себя функцию транспортировки кислорода, предотвращая гипоксию и серповидную деформацию эритроцитов. Обе терапии прошли исчерпывающие клинические исследования для оценки безопасности и эффективности. Стоит отметить, что они требуют предварительной подготовки пациента – так называемого кондиционирования, которое за счёт химиотерапии, радиотерапии или иммуносупрессивных препаратов подавляет иммунитет и костный мозг.

Casgevy был испытан на 45 пациентах, из которых 29 пребывали под наблюдением достаточно долго, чтобы можно было говорить о долговременном эффекте терапии. В частности, 28 из них не имели тяжёлых случаев вазооклюзивного криза как минимум на протяжении 12 месяцев в течении двухлетнего периода наблюдения. Данный метод не вызывает реакции «трансплантат против хозяина» (РТПХ), которая иногда случается при пересадке гемопоэтических стволовых клеток, а в списке побочных эффектов значатся: понижение уровня лейкоцитов, язвы в полости рта, тошнота и рвота, зуд, скелетно-мышечные боли, боль в животе и головная боль. Тем временем терапию Lyfgenia испытали на 32 пациентах, и 88% из них не имели рецидивов кризов в течение 24 месяцев. Увы, применение данного метода повышает риск развития онкологических заболеваний крови: пациенты будут в обязательном порядке получать соответствующее предупреждение и более детальную информацию для отслеживания симптомов.
Casgevy и Lyfgenia признаны методами терапии, способными восполнить неудовлетворённую медицинскую потребность, рассчитанными для лечения орфанных заболеваний. Таковыми считаются заболевания, затрагивающие менее 200 000 человек в пределах юрисдикции США (СКА диагностирована у менее чем 100 000 американцев). Помимо внушительной продолжительности процесса лечения, обусловленной необходимостью кондиционирования пациента и наблюдения после трансплантации модифицированных гемопоэтических стволовых клеток, одним из наиболее существенных недостатков генотерапии является её заоблачная стоимость. По некоторым оценкам, её применения может обходиться в примерно $2 млн на пациента без учёта дополнительных расходов на уход за больным. К тому же FDA требует, чтобы производители продолжали пристальное наблюдение за состоянием пациентов в долгосрочной перспективе, что увеличивает расходы компаний.
